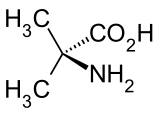
2-Amino-2-methylpropionsäure
| Strukturformel | ||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
 | ||||||||||||||||||||||
| Allgemeines | ||||||||||||||||||||||
| Name | 2-Amino-2-methylpropionsäure | |||||||||||||||||||||
| Andere Namen |
| |||||||||||||||||||||
| Summenformel | C4H9NO2 | |||||||||||||||||||||
| Kurzbeschreibung |
weißes Pulver[1] | |||||||||||||||||||||
| Externe Identifikatoren/Datenbanken | ||||||||||||||||||||||
| ||||||||||||||||||||||
| Eigenschaften | ||||||||||||||||||||||
| Molare Masse | 103,2 g·mol−1 | |||||||||||||||||||||
| Aggregatzustand |
fest | |||||||||||||||||||||
| Dichte |
1,109 g·cm−3[2] | |||||||||||||||||||||
| Schmelzpunkt |
335 °C[3] | |||||||||||||||||||||
| pKS-Wert | ||||||||||||||||||||||
| Löslichkeit |
löslich in Wasser[3] | |||||||||||||||||||||
| Sicherheitshinweise | ||||||||||||||||||||||
| ||||||||||||||||||||||
| Toxikologische Daten | ||||||||||||||||||||||
| Wenn nicht anders vermerkt, gelten die angegebenen Daten bei Standardbedingungen (0 °C, 1000 hPa). | ||||||||||||||||||||||
2-Amino-2-methylpropionsäure ist eine nichtproteinogene Aminosäure. Das α-Kohlenstoffatom ist zudem kein Stereozentrum, die Verbindung ist daher nicht chiral.
Gewinnung
Im Labormaßstab kann 2-Amino-2-methylpropionsäure aus Acetoncyanhydrin und Ammonium bei anschließender Hydrolyse gewonnen werden.[5]
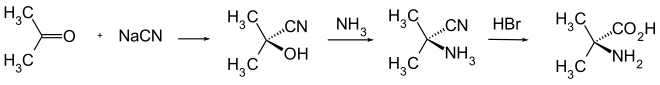
Eigenschaften
Die Sekundärstruktur von Peptiden dieser achiralen Aminosäure kann dadurch beeinflusst werden, welche chirale Aminosäure als N-Terminus angefügt wird. Mit (S)-Valin oder auch (R)-α-Methylvalin bilden sich überwiegend linkshändige 310-Helices aus, mit (S)-α-Methylvalin dagegen rechtshändige. Ursache hierfür ist, dass die β-Schleife vom Typ II, wie sie im Falle von (S)-Valin begünstigt wird, im Falle von (S)-α-Methylvalin durch die ekliptische Konformation der zusätzlichen Methylgruppe destabilisiert wird, sodass bevorzugt eine β-Schleife vom Typ III entsteht, was zu einer rechtshändigen 310-Helix führt.[6] Das Verhältnis der beiden Konformationen beträgt etwa 3:1.[7]
Einzelnachweise
- 1 2 3 Datenblatt α-Aminoisobuttersäure bei Sigma-Aldrich, abgerufen am 23. April 2013 (PDF).
- ↑ 2-amino isobutyric acid. Pharmasi Chemicals Co.,Ltd, abgerufen am 27. Juni 2024.
- 1 2 Datenblatt 2-Aminoisobutyric acid bei Alfa Aesar, abgerufen am 18. Juni 2023 (Seite nicht mehr abrufbar).
- 1 2 W. M. Haynes (Hrsg.): CRC Handbook of Chemistry and Physics. 97. Auflage. (Internet-Version: 2016), CRC Press / Taylor and Francis, Boca Raton FL, Dissociation Constants of Organic Acids and Bases, S. 5-88.
- ↑ Clarke, H. T.; Bean, H. J: α-Aminoisobutyric Acid In: Organic Syntheses. 11, 1931, S. 4, doi:10.15227/orgsyn.011.0004; Coll. Vol. 2, 1943, S. 29 (PDF).
- ↑ Matteo De Poli, Marta De Zotti, James Raftery, Juan A. Aguilar, Gareth A. Morris, Jonathan Clayden: Left-Handed Helical Preference in an Achiral Peptide Chain Is Induced by an l-Amino Acid in an N-Terminal Type II β-Turn. In: The Journal of Organic Chemistry, 2013, Band 78, S. 2248–2255, doi:10.1021/jo302705k.
- ↑ Jordi Solà, Gareth A. Morris, Jonathan Clayden: Measuring Screw-Sense Preference in a Helical Oligomer by Comparison of 13C NMR Signal Separation at Slow and Fast Exchange. In: Journal of the American Chemical Society, 2011, Band 133, S. 3712–3715, doi:10.1021/ja1097034.