Pharmaceutical Inspection Co-operation Scheme
| Pharmaceutical Inspection Co-operation Scheme (PIC/S) | |
|---|---|
| Rechtsform | Internationale Organisation |
| Gründung | 2. November 1995 |
| Sitz | Genf, Schweiz (⊙) |
| Mitglieder | 56 (aus 52 Staaten) |
| Website | https://www.picscheme.org/ |
Das Pharmaceutical Inspection Co-operation Scheme (PIC/S) ist ein internationaler Zusammenschluss von GMP-Überwachungsbehörden als Nachfolgeprogramm der Pharmaceutical Inspection Convention.[1] PIC/S soll zur Verbesserung der Zusammenarbeit von Regulierungsbehörden und Pharmazeutischer Industrie im Bereich der Guten Herstellungspraxis beitragen.
Geschichte
Die Pharmaceutical Inspection Convention wurde im Oktober 1970 von der Europäischen Freihandelsassoziation als Convention for the Mutual Recognition of Inspections in Respect of the Manufacture of Pharmaceutical Products gegründet.[2][3] Gründungsmitglieder waren die damaligen 10 Mitglieder der EFTA. Anfang der 1990er stellte man fest, dass aufgrund einer Inkompatibilität von PIC und Europarecht keine neuen Länder als PIC-Mitglieder aufgenommen werden konnten. Das Europarecht erlaubte es einzelnen EU-Mitgliedsstaaten nämlich nicht, Abkommen mit anderen Staaten zu schließen, die der PIC beitreten wollten. Daher wurde am 2. November 1995 das Pharmaceutical Inspection Co-operation Scheme gegründet. Dabei handelt es sich um eine informelle Vereinbarung zwischen Gesundheitsbehörden und nicht um einen Vertrag zwischen Staaten.[3]
Bis 2003 war PIC/S keine eigene Rechtsperson. Das Sekretariat wurde von der Europäischen Freihandelsassoziation bereitgestellt. Basierend auf einem PIC/S-Treffen im Juni 2003 entschied sich das Komitee, sich selbst als Schweizer Verein nach Artikel 60 des Zivilgesetzbuchs zu konstituieren. Am 1. Januar 2004 hat PIC/S ein eigenes Sekretariat in Genf eingerichtet.[4]
Zweck
PIC/S hat eine Reihe von Bestimmungen, die folgendes erreichen sollen:[5]
- Gegenseitige Anerkennung der Inspektionen zwischen den Mitgliedsländern, sodass eine Inspektion, die von Beamten eines Mitgliedslands durchgeführt wird, von anderen Mitgliedern als gültig anerkannt wird.
- Äquivalente Prinzipien der Inspektionsmethodik, sodass die Inspektoren in jedem Mitgliedsland die gleichen bewährten Vorgehensweisen bei der Durchführung von Inspektionen anwenden.
- Mechanismen zur Ausbildung von Inspektoren.
- Harmonisierung schriftlicher Standards der Guten Herstellungspraxis.
- Kommunikationswege zwischen den Inspektoren/Überwachungsbehörden der Mitgliedsländer.
Mitglieder
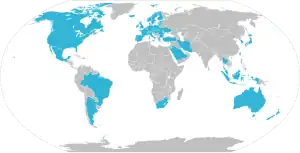
Stand April 2024 hat PIC/S folgende Mitglieder:[6]
| Land | Einrichtung | Beitrittsjahr |
|---|---|---|
| Instituto Nacional de Medicamentos | 2008 | |
| Therapeutic Goods Administration | 1995 | |
| Bundesamt für Sicherheit im Gesundheitswesen | 1999 | |
| Agence Fédérale des Médicaments et des Produits de Santé Federaal Agentschap voor Geneesmiddelen en Gezondheidsproducten | 1997 | |
| Agência Nacional de Vigilância Sanitária | 2021 | |
| Bulgarian Drug Agency | 2023 | |
| Health Canada’s Regulatory Operations and Enforcement Branch Santé Canada Direction générale des opérations réglementaires et de l’application de la loi | 1999 | |
| 食品藥物管理署 | 2013 | |
| Agencija za lijekove i medicinske proizvode | 2016 | |
| Φαρμακευτικές Υπηρεσίες | 2008 | |
| Státní Ústav pro Kontrolu Léčiv Ústav pro státní kontrolu veterinárních biopreparátů a léčiv | 1997 2005 | |
| Lægemiddelstyrelsen | 1995 | |
| Ravimiamet | 2007 | |
| Lääkealan turvallisuus- ja kehittämiskeskus Fimea | 1996 | |
| Agence nationale de sécurité du médicament et des produits de santé Agence nationale de sécurité sanitaire de l’alimentation, de l’environnement et du travail | 1997 2009 | |
| Bundesministerium für Gesundheit
Zentralstelle der Länder für Gesundheitsschutz bei Arzneimitteln und Medizinprodukten |
2000 | |
| Εθνικός Οργανισμός Φαρμάκων | 2002 | |
| 香港藥劑業及毒藥管理局 | 2016 | |
| Országos Gyógyszerészeti és Élelmezés-egészségügyi Intézet | 1995 | |
| Lyfjastofnun | 1995 | |
| Badan Pengawas Obat dan Makanan | 2012 | |
| سازمان غذا و دارو | 2018 | |
| Health Products Regulatory Authority | 1996 | |
| מכון לביקורת ותקנים של חומרי רפואה | 2009 | |
| Agenzia Italiana del Farmaco Direzione generale della sanità animale e dei farmaci veterinari | 2000 2020 | |
| PMDA | 2014 | |
| Zāļu valsts aģentūra | 2004 | |
| Amt für Gesundheit | 1995 | |
| Valstybinė vaistų kontrolės tarnyba | 2009 | |
| Bahagian Regulatori Farmasi Negara | 2002 | |
| Malta Medicines Authority | 2008 | |
| Comisión Federal para la Protección contra Riesgos Sanitarios | 2018 | |
| Inspectie Gezondheidszorg en Jeugd | 1995 | |
| Medsafe | 2013 | |
| Statens legemiddelverk | 1995 | |
| Główny Inspektorat Farmaceutyczny | 2006 | |
| Autoridade Nacional do Medicamento e Produtos de Saúde IP | 1999 | |
| Agenția Națională a Medicamentului și a Dispozitivelor Medicale din România | 1995 | |
| Saudi Food and Drug Authority | 2023 | |
| Health Sciences Authority | 2000 | |
| Státní ústav pro kontrolu léčiv | 1997 | |
| Javna agencija Republike Slovenije za zdravila in medicinske pripomočke | 2012 | |
| South African Health Products Regulatory Authority | 2007 | |
| 대한민국 식품의약품안전처 | 2014 | |
| Agencia Española de Medicamentos y Productos Sanitarios | 1998 | |
| Läkemedelsverket | 1996 | |
| Swissmedic | 1996 | |
| สำนักงานคณะกรรมการอาหารและยา | 2016 | |
| Türkiye İlaç ve Tıbbi Cihaz Kurumu | 2018 | |
| Державна служба України з лікарських засобів та контролю за наркотиками | 2011 | |
| Medicines and Healthcare products Regulatory Agency Veterinary Medicines Directorate | 1999 2014 | |
| Food and Drug Administration | 2011 |
Siehe auch
Weblinks
Einzelnachweise
- ↑ Pharmaceutical Inspection Co-operation Scheme Brochure. (PDF) 2019, abgerufen am 30. Dezember 2021.
- ↑ History of PIC/S. In: picscheme.org. Abgerufen am 2. Oktober 2021.
- 1 2 Daniel Brunner: Pharmaceutical Inspection Co-operation Scheme (PIC/S). In: The Quality Assurance Journal. 8. Jahrgang, Nr. 3, September 2004, S. 207–211 (wiley.com).
- ↑ Legal Form. In: picscheme.org. Abgerufen am 2. Oktober 2021.
- ↑ Kate McCormick: Quality (Pharmaceutical Engineering Series). Butterworth-Heinemann, 2002, ISBN 978-0-7506-5113-4, S. 158.
- ↑ Members. In: www.picscheme.org. Abgerufen am 2. Oktober 2021.